KUVA MITOKONDRIASTA

WIKIPEDIA ANTAA alla HYVÄN KUVAN KOKO SOLUSTA JA TUMASTA, MISSÄ SIGNAALITAPAHTUMIEN RUNKO ON ESITETTYNÄ.
HYVÄÄN TOIMINTAAN KUULUU VAHINGOLLISTEN SIVUTUOTTEIDEN DETONOIMINEN, JÄTTEEN HÄVITYS, DNA:N JA PROTEIINIEN KORJAUS JA OKSIDATIIVINEN REDOX TASAPAINO, MUTTA JOKAINEN YKSITTÄINEN TAPAHTUMA ON ERIKSEEN KATSOTTAVA. Alemmassa kuvassa taas ei näy mitokondria vaan solu ja tuma.
APOPTOOSIIN JOHTAVA TIE JA p53 näkyy kuvassa:
http://en.wikipedia.org/wiki/Signal_transduction#Redox_signaling
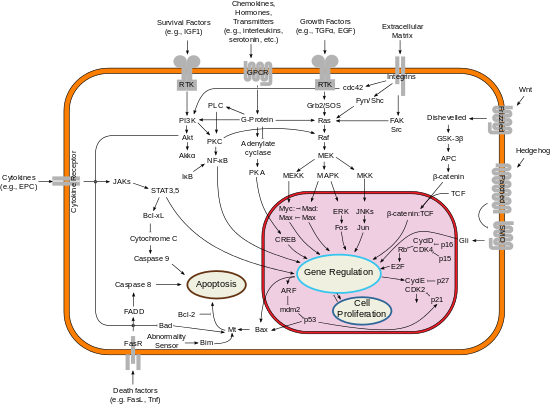
NORMAALI APOPTOOSI
Lähde Björkhem Bergman Linda.
Thioredoxin reductase and selenium in
carcinogenesis and multidrug resistance.
Karolinska Institutet 2004
ISBN917349-954-4.
“Apoptoosi on solun ohjelmoitu kuolema. Siinä prosessissa
tapahtuu monimutkainen tarkasti säädelty solun sisäisten
tapahtumien sarja, kaskadi, joka johtaa solun kuolemaan sen oman
ohjelman johdosta. Apoptoosi sana tulee kreikasta ja tarkoitta
poistippumisa viitaten siihen samantapaiseen ilmiöön kuin puu
tiputtaa lehtiään tietyssä olosuhteessa. Solun nekroottisesa
kuolemassa silloin kun solua on kohdannut vaurio, vapautuu solun
sisältö sen ulkopuolelle ja aiheuttaa tulehdusreaktion, mutta solun
apoptoottisessa kuolemassa ei aiheudu mitään tulehduksellista
vastetta ulospäin.
Apoptoosi on aktiivi. Se kuluttaa ATP-energiaa. Prosessiin liittyy
solun kutistuminen, Sytokromi c erkanee mitokondriasta, Cyt c
on happimolekyylin vastaanottaja. Solu “huokaisee henkensä pois”
, kun sytokromi irtoaa sen energiatehtaasta. Kromatiiniaines
kondensoituu, tiivistyy, DNA fragmentoituu, pirstoutuu ja plasmakalvo
alkaa kupruilla, rakkuloitua ja lopultaa muodostuu apoptoottisia
hiukkasia siitä mikä oli elävä solu. Koska mitään jätettä ei
vuoda solun ulkopuolelle, vältytään kudoksen tulehdukselta.
Fagosytoivia soluja ei ole havaittavissa soluviljelmissä, jotka ovat
keinotekoisia malleja tutkittaessa apoptoosia ja siten tapahtuu
sekundäärinen nekroosi.
Apoptoosi on luonnollisesti hyvin tärkeä prosssi
normaalissa ihmisalkion kehityksessä, sillä sen avulla sorvautuu
esiin hienot piirteet ja jäsenet, kuten sormet ja varpaat. Kudos
tasapainossa, homeostaasissa normaalin solunudistumisen ja
solukuolemans kesken apoptoosilla on pääosa. Esimerkiksi
vertamuodostavan kudoksen täytyy omata normaali apoptoosi, jossa
päivittäin katoaa tuhansia miljoonia valkosoluja. Jos tämä
apoptoosi ei toimisi normaalisti (dysregulaatio) seuraisi
useitasairaustiloja kuten autoimmuniteettia ja neurodegeneratiivisia
sairauksia. Useimmissa syöpäsoluissa on apoptoottista koneistoa
vikuuttavia mutaatioita taustalla.
On kuvattu useita apoptoottisia signaaliteitä. Apoptoottinen
prosessihan on hyvin monimutkainen. Monet solunsisäisten
reaktioitten kaskadit ovat keskenään interaktiossa. Siitä
huolimatta pystytään useinkin erottamaan apoptoosisignaaleissa
kaksi pääryhmää: sisäinen tie välittyy mitokondriasta käsin ja
ulkoinen tie välittyy ligandin kiinnittymisestän solun joihinkin
kuolonreseptoreista.
Entsyymiperhe kaspaasit on hyvin tiiviisti mukana apoptoottisessa
solusignaloinnissa ja vastaa apoptoosin lopullisista exekutiivisista
askeleista. . On kuvattu myös kaspaasista riippumatonta apoptoosia.
Näkökohta apoptoosista ja syöpäterapioista
Syövän lääkehoidon tarkoituksena on triggeröidä syöpäsolussa
esiin tuumoriselektiivinen apoptoosi. Useimmat kemoterapeuttiset
aineet kuten säteilykin vaikuttavat kaspaasista riippuvan apoptoosin
ja p53-välitteisen apoptoosin induktion suspekteissa
soluissa. Mutta pahanlaatuisen solun kyky kiertää ja välttää
apoptoosi on juuri osa tästä karsinogeenisestä prosessista.
Monilla syöpäsoluilla on juuri kaspaasia aktivoivissa teissään
toiminnan häiriötä ja niillä voi olla mutatoitunut p53 geeni (
the guardian of genome).Näinpä moni syöpäsolu on resistentti,
vastustuskykyinen syöpäterapialle tai selektion kautta
kehittää resistenssin.
Kaspaasista riippumaton apoptoositie onkin alkanut herättää
huomiota mahdollisena parempana kohteena syöpäterapialle. Tämän
alternatiivisen tien toiminnanhäiriöt syöpäsoluilla eivät näytä
olevan niin tavallisia kuin klassisen kaspaasista riippuvan tien
dysfunktiot. Mutta optimaalinen syöpäterapia vaatii mahdollisesti
kuitenkin usean solukuolemaan johtavan, toisistaan riippumattoman
tien aktivaatiota, jotta saataisiin paremmaksi vatustuskykyisiä
syöpäsoluja tuhoava vaikutus.”
